Manejo y Corrección de la Acidez de los Suelos
¿Qué es la acidez del suelo?
En la solución del suelo, las altas concentraciones de Aluminio (Al3+) e Hidrógeno activo (H+) dan lugar a la acidez del suelo. El pH (potencial de hidrógeno) es la medida del grado de acidez o alcalinidad de un suelo. Un pH de 7.0 indica neutralidad, pero a medida que este valor disminuye el suelo se vuelve más ácido, de manera que, un pH de 6.0 es diez veces más ácido que un pH de 7.0. El significado práctico del pH en términos de acidez del suelo, es que afecta significativamente la disponibilidad y la asimilación de nutrientes, y ejerce una fuerte influencia sobre la estructura del suelo.

¿Cómo se genera?
Remoción de nutrientes por los cultivos. Los cultivos, sobre todo los de alto rendimiento pueden ocasionar acidez al suelo mediante la absorción de cationes básicos (Ca, Mg y K). La planta, al absorber cationes libera hidrógeno para mantener el equilibrio en su interior, el cual genera acidez. Por ejemplo un cultivo de maíz puede remover hasta 60 kg de Mg ha-1.
Elevada precipitación. El exceso de lluvias ocasiona la lixiviación o lavado de cationes intercambiables (Ca, Mg, K y Na). El potasio y sodio son los dos cationes que se lixivian más fácilmente y dan lugar a ser sustituidos por el hidrógeno y el aluminio.
Descomposición de la materia orgánica.Al descomponerse la materia orgánica por la acción de los microorganismos del suelo, se libera dióxido de carbono que se transforma fácilmente en bicarbonato, esta reacción libera hidrógeno que acidifica el suelo.
Uso de fertilizantes nitrogenados de reacción ácida. Los fertilizantes nitrogenados que contienen o forman amonio (NH4+) incrementan la acidez del suelo. El sulfato de amonio, nitrato de amonio y la urea son los fertilizantes típicos que generan esta reacción. Al aplicar estos fertilizantes al suelo, el amonio (NH4+) se transforma en nitrato (NO3-) gracias a la acción biológica y libera hidrógeno que acidifica el suelo. Esta reacción es necesaria y se da de manera natural, ya que la mayor parte del nitrógeno que absorbe la planta es en forma de nitrato. Por cada molécula de NH4 que se transforma a NO3, se liberan dos moléculas de H+.
Aluminio intercambiable. La presencia de aluminio (Al3+) en la solución del suelo induce el desarrollo de la acidez del suelo. El aluminio que se desplaza de las arcillas por otros cationes reacciona con el agua y libera hidrógenos. Este incremento en la acidez promueve la presencia de más aluminio disponible para reaccionar nuevamente. Tan solo una concentración de 2-5 ppm de aluminio en la solución de suelo es tóxica para cultivos sensibles, y más de 5 ppm ya es tóxico para cultivos tolerantes.

¿Qué efectos causa?
La producción de cultivos en suelos ácidos impide conseguir altos potenciales de rendimiento y buena calidad de las cosechas (Cuadro 2), por ejemplo, en muchas regiones de México y Centroamérica la productividad del maíz ha disminuido por efecto de la acidez. En estas condiciones del suelo, la solubilidad del aluminio (Al), hierro (Fe) y manganeso (Mn) es elevada y sus concentraciones aumentan hasta llegar a niveles muy tóxicos para las plantas. Por su parte, el aluminio también impide la absorción de calcio y magnesio. Finalmente, las raíces se acortan y engrosan, impidiendo así la absorción de agua y nutrimentos, en particular, el abasto de fosforo (P) y molibdeno (Mo) se ve seriamente comprometido. Sin embargo, el efecto más grave es sobre el proceso de fijación biológica de nitrógeno en las leguminosas.

¿Dónde se presenta?
En México, los suelos ácidos se encentran distribuidos en las regiones tropicales y en los bosques templados. Se sabe que cubren una superficie cercana a los 14 millones de ha, donde Veracruz, Tabasco, Chiapas y Campeche son los estados que concentran la mayor cantidad de suelos con estas características. Por ejemplo, una de las regiones más afectadas por la acidez del suelo es la Frailesca, en el Estado de Chiapas. Sin embargo en estados como Jalisco, Nayarit y Colima, también hay muchas zonas con suelos ácidos.
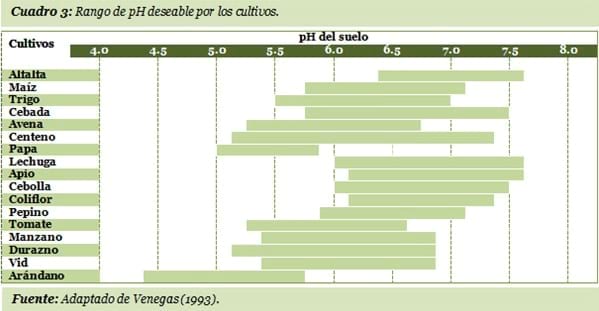
¿Qué pH prefieren los cultivos?
Los cultivos tienen un rango de pH en el cual se desarrollan adecuadamente, pero a medida que se sale de estos valores sus rendimientos se ven afectados.
¿Cómo se mide?
Uno de los principales objetivos de análisis de suelos es conocer el pH del mismo. A partir del conocimiento de este parámetro se determina si hay que adicionar mejoradores de suelo que disminuyan este problema. El uso del potenciómetro es el método más preciso y utilizado para esta determinación, puede hacerse en laboratorio, aunque actualmente ya existen equipos portátiles que miden el pH con tanta precisión como los de laboratorio. El valor de pH del suelo se determina al poner en contacto una suspensión suelo-agua destilada (en una relación 1:2 o 1:1), pero también se suele medir usando CaCl20.01M o KCl 1 N en lugar de agua. La determinación de pH en CaCl2 es normalmente 0.5 a 0.8 unidades más baja que la determinada usado agua solamente. Cuando la medición de pH se realiza en una solución de KCl 1 N, la diferencia en pH con respecto al medido en agua pude llegar a ser más de una unidad más baja que en agua. Por esta razón, cuando se reporta el pH del suelo, siempre se debe indicar el procedimiento de determinación y la relación suelo:agua o solución empleada, para poder interpretar el dato correctamente. En lo sucesivo cuando se especifique el pH del suelo, nos referimos al medido en suelo:agua (1:2), dado que es la que se usa mayormente.

¿Cómo se controla?
Aunque en la actualidad se disponga de genotipos tolerantes a la acidez, la solución más acertada, técnica y económicamente, es la aplicación de materiales básicos (enmiendas calcáreas) que neutralicen la acidez. Esta práctica se conoce como encalado y los materiales que la hacen posible son principalmente carbonatos, óxidos, hidróxidos y silicatos de calcio y/o magnesio, todos con diferente capacidad de neutralización.
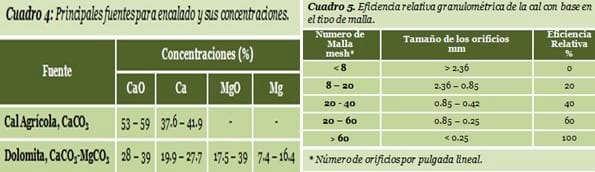
¿Qué productos se deben de usar?El material más utilizado para el encalado de suelos es la cal agrícola o calcita, la cual contiene principalmente carbonato de calcio (CaCO3). El óxido de calcio (CaO) conocido como cal viva y el hidróxido de calcio [Ca (OH)2] conocido como cal hidratada, son dos fuentes de rápida reacción en el su suelo, pero muy difíciles y desagradables de manejar, por lo que no se recomienda su uso. Otras fuentes como la dolomita (CaCO3. MgCO3) tienen la ventaja de aportar magnesio. La calidad de estos materiales se establece principalmente en base a los siguientes términos:
Pureza del material. La capacidad para neutralizar la acidez depende de la pureza y composición química de la fuente. Para conocer la pureza se utiliza el criterio del equivalente químico (EQ) que es la medida del poder de neutralización de una cal en particular. Su capacidad para neutralizar se compara con el poder de neutralización del CaCO3 químicamente puro, al cual se le asigna un valor de 100 %. Los materiales con menos de 80 % de EQ (32 % de Ca) son de baja calidad.
Tamaño de las partículas. La velocidad de reacción de los materiales se determina por el tamaño de sus partículas. A menor tamaño de partícula hay mayor superficie de contacto con el suelo (mayor superficie específica), por lo tanto mayor rapidez de reacción.
Poder relativo de neutralización total (PRNT). Es la evaluación conjunta de la pureza y finura de los materiales. Este índice de eficiencia se obtiene multiplicando la eficiencia granulométrica por el equivalente químico y este producto se divide entre 100.
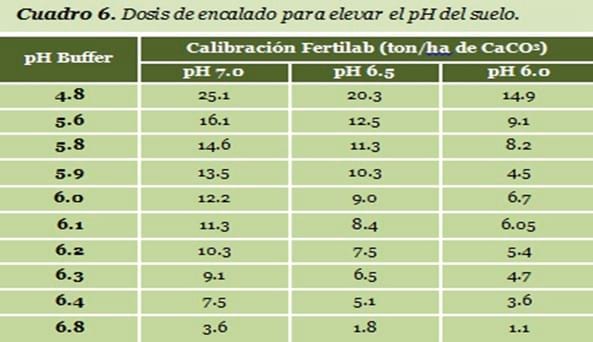
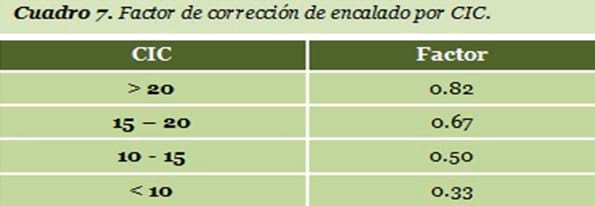
¿Qué dosis de encalado aplicar al suelo?Los suelos difieren en su capacidad de amortiguamiento (oponerse a un cambio de pH). Normalmente los suelos con mayor contenido de materia orgánica y arcilla tienen mayor capacidad de amortiguamiento, por lo tanto requieren mayor cantidad de enmienda para un cambio de pH. Esta característica de los suelos depende de su capacidad de intercambio catiónico (CIC). Para saber los requerimientos de cal se determina la capacidad de amortiguamiento del suelo mediante una determinación llamada pH Buffer. A través de esta determinación Se ha calibrado las dosis de encalado, ajustadas en función del valor de la CIC. El dato de dosis de encalado del cuadro 6 debe de ser ajustado en base a la CIC del suelo, según los valores que se indican en el cuadro 7.
¿Cómo y cuándo aplicar la cal?La cal se mueve muy poco en el suelo, de manera que sus efectos benéficos ocurren solamente en la zona de aplicación. La efectividad de la cal se logra mezclando perfectamente el material en los primeros 15 – 20 cm de suelo utilizando implementos como la rastra. La incorporación del material asegura mayor eficiencia, sobre todo en suelos de textura media a pesada. Para cultivos ya establecidos o pastos, y cultivos perennes, la incorporación no es posible y la única forma de aplicación es superficial o con escasa incorporación. En cultivos como café, plátano y palma aceitera, la aplicación se realiza en banda o en zona de fertilización.
Para que la reacción química se manifieste es necesario que haya humedad en el suelo, de tal manera que el encalado se lleva a cabo unos dos meses antes de la temporada de lluvias para mayor efectividad.
¿Con que frecuencia encalar?Conocer el ritmo de acidificación o alcalinización a través del estudio del suelo nos permite definir la frecuencia, tipo y cantidad de cal a aplicar. Lamentablemente no es muy certero hacer generalizaciones respecto a la frecuencia de encalado, ya que son muchos los factores involucrados, tales como la capacidad de amortiguamiento del suelo, la precipitación pluvial, el uso de fertilizantes amoniacales, y la incorporación de materia orgánica.
Conocer el ritmo de acidificación o alcalinización a través del estudio del suelo nos permite definir la frecuencia, tipo y cantidad de cal a aplicar. Lamentablemente no es muy certero hacer generalizaciones respecto a la frecuencia de encalado, ya que son muchos los factores involucrados, tales como la capacidad de amortiguamiento del suelo, la precipitación pluvial, el uso de fertilizantes amoniacales, y la incorporación de materia orgánica.
Uso del yeso agrícola como enmiendaEl yeso agrícola (sulfato de calcio dihidratado) también se emplea como enmienda en suelos ácidos, pero únicamente como un mejorador del ambiente radicular, ya que por ser una sal neutra su aplicación no cambia la acidez del suelo (prácticamente no hay cambio en el pH). Es un material que aporta calcio y azufre, disminuye la actividad del aluminio en el suelo, reduce la saturación de aluminio en el complejo de intercambio en el suelo, favorece el crecimiento y una mayor exploración de raíces, y crea una mejor estructura del suelo.
En la solución del suelo, las altas concentraciones de Aluminio (Al3+) e Hidrógeno activo (H+) dan lugar a la acidez del suelo. El pH (potencial de hidrógeno) es la medida del grado de acidez o alcalinidad de un suelo. Un pH de 7.0 indica neutralidad, pero a medida que este valor disminuye el suelo se vuelve más ácido, de manera que, un pH de 6.0 es diez veces más ácido que un pH de 7.0. El significado práctico del pH en términos de acidez del suelo, es que afecta significativamente la disponibilidad y la asimilación de nutrientes, y ejerce una fuerte influencia sobre la estructura del suelo.

Remoción de nutrientes por los cultivos. Los cultivos, sobre todo los de alto rendimiento pueden ocasionar acidez al suelo mediante la absorción de cationes básicos (Ca, Mg y K). La planta, al absorber cationes libera hidrógeno para mantener el equilibrio en su interior, el cual genera acidez. Por ejemplo un cultivo de maíz puede remover hasta 60 kg de Mg ha-1.
Elevada precipitación. El exceso de lluvias ocasiona la lixiviación o lavado de cationes intercambiables (Ca, Mg, K y Na). El potasio y sodio son los dos cationes que se lixivian más fácilmente y dan lugar a ser sustituidos por el hidrógeno y el aluminio.
Descomposición de la materia orgánica.Al descomponerse la materia orgánica por la acción de los microorganismos del suelo, se libera dióxido de carbono que se transforma fácilmente en bicarbonato, esta reacción libera hidrógeno que acidifica el suelo.
Uso de fertilizantes nitrogenados de reacción ácida. Los fertilizantes nitrogenados que contienen o forman amonio (NH4+) incrementan la acidez del suelo. El sulfato de amonio, nitrato de amonio y la urea son los fertilizantes típicos que generan esta reacción. Al aplicar estos fertilizantes al suelo, el amonio (NH4+) se transforma en nitrato (NO3-) gracias a la acción biológica y libera hidrógeno que acidifica el suelo. Esta reacción es necesaria y se da de manera natural, ya que la mayor parte del nitrógeno que absorbe la planta es en forma de nitrato. Por cada molécula de NH4 que se transforma a NO3, se liberan dos moléculas de H+.
Aluminio intercambiable. La presencia de aluminio (Al3+) en la solución del suelo induce el desarrollo de la acidez del suelo. El aluminio que se desplaza de las arcillas por otros cationes reacciona con el agua y libera hidrógenos. Este incremento en la acidez promueve la presencia de más aluminio disponible para reaccionar nuevamente. Tan solo una concentración de 2-5 ppm de aluminio en la solución de suelo es tóxica para cultivos sensibles, y más de 5 ppm ya es tóxico para cultivos tolerantes.

La producción de cultivos en suelos ácidos impide conseguir altos potenciales de rendimiento y buena calidad de las cosechas (Cuadro 2), por ejemplo, en muchas regiones de México y Centroamérica la productividad del maíz ha disminuido por efecto de la acidez. En estas condiciones del suelo, la solubilidad del aluminio (Al), hierro (Fe) y manganeso (Mn) es elevada y sus concentraciones aumentan hasta llegar a niveles muy tóxicos para las plantas. Por su parte, el aluminio también impide la absorción de calcio y magnesio. Finalmente, las raíces se acortan y engrosan, impidiendo así la absorción de agua y nutrimentos, en particular, el abasto de fosforo (P) y molibdeno (Mo) se ve seriamente comprometido. Sin embargo, el efecto más grave es sobre el proceso de fijación biológica de nitrógeno en las leguminosas.

En México, los suelos ácidos se encentran distribuidos en las regiones tropicales y en los bosques templados. Se sabe que cubren una superficie cercana a los 14 millones de ha, donde Veracruz, Tabasco, Chiapas y Campeche son los estados que concentran la mayor cantidad de suelos con estas características. Por ejemplo, una de las regiones más afectadas por la acidez del suelo es la Frailesca, en el Estado de Chiapas. Sin embargo en estados como Jalisco, Nayarit y Colima, también hay muchas zonas con suelos ácidos.
Los cultivos tienen un rango de pH en el cual se desarrollan adecuadamente, pero a medida que se sale de estos valores sus rendimientos se ven afectados.

Uno de los principales objetivos de análisis de suelos es conocer el pH del mismo. A partir del conocimiento de este parámetro se determina si hay que adicionar mejoradores de suelo que disminuyan este problema. El uso del potenciómetro es el método más preciso y utilizado para esta determinación, puede hacerse en laboratorio, aunque actualmente ya existen equipos portátiles que miden el pH con tanta precisión como los de laboratorio. El valor de pH del suelo se determina al poner en contacto una suspensión suelo-agua destilada (en una relación 1:2 o 1:1), pero también se suele medir usando CaCl20.01M o KCl 1 N en lugar de agua. La determinación de pH en CaCl2 es normalmente 0.5 a 0.8 unidades más baja que la determinada usado agua solamente. Cuando la medición de pH se realiza en una solución de KCl 1 N, la diferencia en pH con respecto al medido en agua pude llegar a ser más de una unidad más baja que en agua. Por esta razón, cuando se reporta el pH del suelo, siempre se debe indicar el procedimiento de determinación y la relación suelo:agua o solución empleada, para poder interpretar el dato correctamente. En lo sucesivo cuando se especifique el pH del suelo, nos referimos al medido en suelo:agua (1:2), dado que es la que se usa mayormente.

Aunque en la actualidad se disponga de genotipos tolerantes a la acidez, la solución más acertada, técnica y económicamente, es la aplicación de materiales básicos (enmiendas calcáreas) que neutralicen la acidez. Esta práctica se conoce como encalado y los materiales que la hacen posible son principalmente carbonatos, óxidos, hidróxidos y silicatos de calcio y/o magnesio, todos con diferente capacidad de neutralización.
Tamaño de las partículas. La velocidad de reacción de los materiales se determina por el tamaño de sus partículas. A menor tamaño de partícula hay mayor superficie de contacto con el suelo (mayor superficie específica), por lo tanto mayor rapidez de reacción.
Poder relativo de neutralización total (PRNT). Es la evaluación conjunta de la pureza y finura de los materiales. Este índice de eficiencia se obtiene multiplicando la eficiencia granulométrica por el equivalente químico y este producto se divide entre 100.

Para que la reacción química se manifieste es necesario que haya humedad en el suelo, de tal manera que el encalado se lleva a cabo unos dos meses antes de la temporada de lluvias para mayor efectividad.

Conocer el ritmo de acidificación o alcalinización a través del estudio del suelo nos permite definir la frecuencia, tipo y cantidad de cal a aplicar. Lamentablemente no es muy certero hacer generalizaciones respecto a la frecuencia de encalado, ya que son muchos los factores involucrados, tales como la capacidad de amortiguamiento del suelo, la precipitación pluvial, el uso de fertilizantes amoniacales, y la incorporación de materia orgánica.

Cambiar el PH podemos incurrir en otros problemas que refieren a la relación de los macronutrientes.
En otras palabras, un suelo que esté desequilibrado en sus bases (relación Ca/Mg/Na/K/H) va a sufrir cambios en el PH. Encalar par cambiar el PH es atacar la consecuencia y no la causa.
Creo que el foco debe ponerse en diagnosticar adecuadamente con un laboratorio confiable, la situación de los macronutrientes que integran la CIC y descubrir la relación entre ellos. Una vez que se tiene este diagnóstico, se puede prescribir las enmiendas necesarias (que nutriente, en que cantidad y con que granulometría) . Al reestablecer ese equilibrio, el PH se moverá hacia su justa medida para el suelo en cuestión (que como usted bien indica, será diferente si es arenoso, o arcilloso, etc).
Respecto de la granulometría, no tengo dudas que es esencial, lo que vemos normalmente en Uruguay son enmiendas calcáreas demasiado gruesas. Estas reaccionan con el tiempo con el suelo y no nos da predescibilidad. Al menos un 80% del material debe pasar malla 60, en mi concepto.
En la Clinica del Suelo, estamos trabajando en este tema, tratando de llegar en profundidad a determinar cual es el punto de partida. Es igual a ir al médico para que nos practique un examen completo y exhaustivo. La mayoría de nosotros no lo hacemos y muchos "no quieren saber". Este segundo aspecto es preocupante porque anticipa que sabemos que tenemos un problema, que es complejo de resolver, que seguramente no sea barato y algunos prefieren mirar para otro lado.
Cuando logramos equilibrar los macronutrientes del suelo, hemos probado el uso de microorganismos como forma de ayudar a sostener lo logrado y ha funcionado muy bien. Esta tecnología muchas veces fracasa porque el suelo está desordenado químicamente.
El yeso agrícola es un complemento del control de la acidez de los suelos, la cal agrícola, actua en los primeros 20 cm aproximadamente, el yeso agrícola, con el ion sulfato actua en el subsuelo bloqueando la acción toxica del aluminio y otros metales. Este efecto favorece al desarrollo de la raíz y de la planta, con ph, superiores a 5.8, el efecto bloqueante del yeso agrícola sobre el aluminio toxico, que se acumula en el subsuelo, produce mayor impacto que la misma aplicación de cal, que conlleva complicados movimientos de suelos y mayores riesgos de erosion, en cambio, el yeso actua y decsiende por el perfil, desde la superficie.
La Zeolita una vez estabilizado el suelo químicamente, actua con una elevada capacidad de captación de cationes, aniones y agua, permitiendo aumentar los nutrientes de fácil disponibilidad para el vegetal en crecimiento. Esto se lo da su enorme superficie de adsorción. pero es inerte químicamente. En un suelo àcido el bloqueo de nutrientes impide el accionar de la Seolita,
Fertilidad del Suelo
El Análisis de un suelo es para conocer la capacidad de suministrar nutrientes minerales esenciales para las plantas.
Hay Factores que afectan al suministro de nutrientes a las plantas Uno puede administrar los nutrientes a las plantas , en base a los análisis, que a su vez mejora la fertilidad.
TABLA 1 - ELEMENTOS ESENCIALES DE NUTRIENTES Y SUS FUENTES
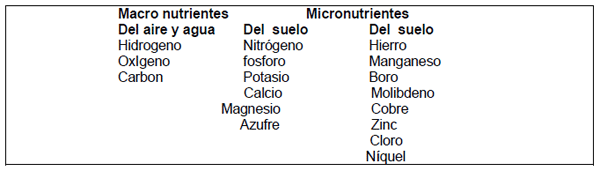
Elementos necesarios en cantidades relativamente grandes se conocen como macro nutrientes, mientras que las que se necesitan en cantidades relativas más pequeñas se conocen como micronutrientes, o elementos traza. Los micronutrientes son más propensos a ser un problema en :
a) Suelos arenosos
b) Suelos orgánicos
c) Suelos muy alcalinos
b) Suelos orgánicos
c) Suelos muy alcalinos
La causa de esto es debido a las cantidades relativamente pequeñas en las arenas , suelos orgánicos y baja disponibilidad en suelos alcalinos.
De los macro nutrientes, N, P, y K se llaman los elementos primarios, mientras que Ca, Mg, y S se consideran elementos secundarios.
C, H, y O componen aproximadamente el 95% de una planta. Los elementos minerales se obtienen, naturalmente, de la erosión de los minerales primarios y secundarios del suelo, la biodegradación de la materia orgánica, y gases en la atmósfera. Estas fuentes naturales se complementan con los fertilizantes, abonos y humus.
Elementos esenciales y las principales formas en que son absorbidos por las raíces de las plantas.

Por lo general, sólo una pequeña cantidad de un elemento está disponible en la solución del suelo, mientras que una gran cantidad se adsorbe sobre las partículas del suelo. La disponibilidad se relaciona con muchos factores del suelo y cantidad presente.
DISPONIBILIDAD DE NUTRIENTES VEGETALES
Los nutrientes se encuentran en el suelo en :
A.-Formas no disponibles de nutrientes
B.-Materia orgánica del suelo
C.-Compuestos precipitados.
B.-Materia orgánica del suelo
C.-Compuestos precipitados.
Los factores que afectan a la conversión de no disponible a las formas disponibles y viceversa son
La actividad microbiana se ve afectada por la humedad, la aireación, el suministro de nutrientes, temperatura, y pH del suelo.
La transferencia de iones disponibles a la superficie de la raíz se ve afectada por la cantidad de iones intercambiables, y por el gradiente de concentración (cantidad) presente de iones disueltos.
ABSORCION DE SUSTANCIAS NUTRITIVAS
La absorción de nutrientes de la planta se rige por el suministro de nutrientes disponibles y por la concentración de ese elemento en superficies de la raíz de la planta. Los nutrientes se suministran a las raíces de tres maneras.
En primer lugar, las raíces penetran en el suelo y entran en contacto directo con los coloides del suelo y los nutrientes que contienen los coloides. Esto se conoce como la intercepción de la raíz.
En segundo lugar, algunos nutrientes en la solución del suelo pueden moverse a la raíz con el agua a través de flujo de masa.
En tercer lugar, algunos nutrientes se mueven en respuesta a gradientes de concentración entre la zona de la raíz inmediata y zonas de suelos más alejados. Esto se llama de difusión.
En segundo lugar, algunos nutrientes en la solución del suelo pueden moverse a la raíz con el agua a través de flujo de masa.
En tercer lugar, algunos nutrientes se mueven en respuesta a gradientes de concentración entre la zona de la raíz inmediata y zonas de suelos más alejados. Esto se llama de difusión.
Las plantas toman el nitrógeno principalmente por flujo de masa, por difusión el fósforo, y potasio por difusión.
Solubilidad de nutrientes
La Solubilidad de nutrientes se ve afectada por exudados de las raíces y la actividad microbiana, cerca de la raíz. Una vez solubilizado, hay entrada de nutrientes en la raíz Y la cual se ve afectada y reducida por:
En primer lugar, si el oxígeno está limitado se reduce la velocidad de absorción.
En segundo lugar, las bajas temperaturas limitan la respiración y por lo tanto las tasas de absorción lenta.
En segundo lugar, las bajas temperaturas limitan la respiración y por lo tanto las tasas de absorción lenta.
PH del Suelo
La acidez o alcalinidad del suelo se mide por un medidor de pH.
Un pH del suelo de 7.0 es neutral y es ácido por debajo o por encima es alcalino.
El PH del suelo influye directamente para la Biodisponibilidad de los nutirentes para la planta y desarrollo de micro organismos en el suelo.

MATERIA ORGÁNICA Y SU IMPORTANTANCIA EN LA FERTILIDAD DEL SUELO
Influye en las propiedades físicas y químicas de los suelos. En algunos suelos puede ser responsable de casi la mitad de la capacidad de intercambio catiónico (CIC).
Los microbios en el suelo también utilizan el M.O. como una fuente de alimento.
Tres reacciones generales se producen en el suelo después de la adición de los tejidos orgánicos:
- Aumenta la oxidación enzimática
- N, P, y S son mineralizada y / o inmovilizado
- Los compuestos resistentes a la degradación se forman ya sea a partir de compuestos presentes en los tejidos de las plantas originales o por síntesis microbiana
La materia orgánica disminuye con quema de residuos de los cultivos.
El contenido de materia orgánica disminuirá en situaciones donde el suelo es más aireada y donde los suelos carecen de fertilidad. La rotación de cultivos con leguminosas ayuda a mantener la materia orgánica del suelo debido a la menor labranza y aireación.
Así como la aplicación de materias orgánicas.( compostas , siembras para incorporar en verde).
CAPACIDAD DE INTERCAMBIO CATIÓNICO ( C.I.C.)
Es la capacidad que tiene el suelo de retener e intercambiar cationes. La fuerza de la carga positiva varía dependiendo del catión, permitiendo que un catión reemplace a otro en una partícula de suelo cargada negativamente.
Cationes son los nutrientes, iones y moléculas cargados positivamente. Los principales cationes en el suelo son: calcio (Ca), magnesio (Mg), potasio (K), sodio (Na), hidrógeno (H) y amonio (NH4). Las partículas de arcilla son los constituyentes del suelo cargados negativamente. Estas partículas cargadas negativamente (arcillas), retienen y liberan nutrientes cargados positivamente (cationes). Las partículas de materia orgánica también están cargadas negativamente y también atraen cationes.
Las partículas de arena son inertes (sin carga) y no reaccionan
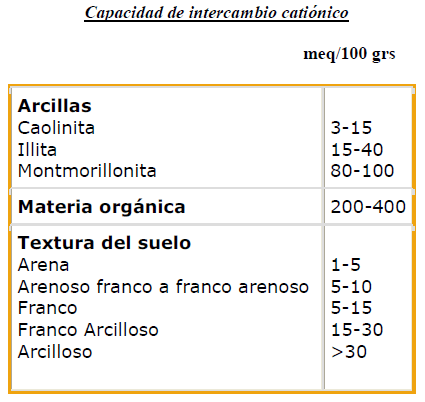
A medida que el contenido de arcilla y/o materia orgánica aumentan el suelo en cuestión tendrá mayor CIC.
Esta capacidad de retener e intercambiar cationes es un indicador directo de la fertilidad de los suelos.
Suelos de textura gruesa (arenosos) poseen una CIC menor, por lo tanto los cationes son retenidos sólo en una baja proporción.
Los microorganismos del suelo
El suelo es el anfitrión de una gran población de organismos vivos.
Casi todos los microorganismos (o microbios) se encuentran en los 75 centímetros de tierra, y la mayoría se concentran en la parte superior a varios centímetros. La población de bacterias, por ejemplo, puede ser más de cuatro veces mayor en los tres primeros centímetros de suelo que en los 40 centímetros.
La mayoría de los microbios obtener alimentos y energía al descomponer sustancias orgánicas complejas proporcionadas por las plantas y animales superiores.
Varios microbios crecen mejor bajo diferentes condiciones:
Bacterias - prefieren un buen drenaje, cerca de los suelos de pH neutro, temperaturas moderadas y buena aireación
Hongos - prefieren suelos ácidos
La descomposición de la materia orgánica completa un ciclo importante en el mundo de las plantas. Cuando una planta crece, absorbe los nutrientes del suelo, madura y muere; luego a través de la descomposición microbiana, los nutrientes son liberados y puestos a disposición para la siguiente generación de nuevo. Sin este proceso, la mayor parte del carbono en el medio ambiente sería atado en el tejido vegetal y animal. Durante la descomposición, ciertos ácidos se forman que reaccionan con los minerales del suelo que contienen elementos vitales de la planta; esto los hace más soluble y disponible para las plantas en crecimiento. Volviendo residuos al suelo suministra los materiales orgánicos necesarios para mantener el proceso continuo.
Los residuos vegetales, no podrán contener suficiente nitrógeno para satisfacer las "dietas" de los microbios. En este caso, pueden consumir el carbono de los residuos y el nitrato disponible en el suelo. Su consumo puede ser tan grande, que poco queda para el cultivo. Esto se conoce como la inmovilización biológica.
Los microbios funcionan mejor si la relación de carbono a nitrógeno (relación C: N) es menor que 25:1. Cuando la relación es mayor de 25:1, los microbios tienen que pedir prestado N del suelo para completar su tarea.
Fosforo en el suelo
El fósforo (P) se derivado de la materia orgánica y minerales del suelo. Se absorbe activamente por raíces de las plantas principalmente como H2PO4- o HPO4 -.
La disponibilidad de fósforo en los suelos es mayor cuando el pH del suelo es de entre 5,5 y 7,0.
Los síntomas de deficiencia de fósforo en el campo son difíciles de interpretar porque no hay síntomas externos específicos.
Deficiencias fósforo en maíz se caracterizan por, retraso del crecimiento, lento y de color verde oscuro. A veces las hojas inferiores y los tallos tienen una tendencia a volverse de color púrpura.
Legumbres.-Los principales síntomas de la deficiencia de fósforo son una tasa de retraso del crecimiento, con hojas de color verde oscuro o cambiando a verde azulado y floración Errática.
La mineralización del P orgánico en relación con el directorio C: N: P sugiere que cuando la relación C: P inorgánico es 200:1 o menos, la mineralización se producirá. Si esa proporción es de 300:1 o más inmovilización se producirá.
AZUFRE DEL SUELO
El azufre (S) es un constituyente de la metionina y cistina aminoácidos, además de la biotina y vitaminas tiamina. Es esencial para el crecimiento de plantas.
La inmovilización se produce cuando se añaden materiales orgánicos como residuos de cultivos para suelos de baja en S. inorgánico .
Sulfato es un anión y es, por tanto, débilmente unida a los sitios de intercambio del suelo y se lixivia fácilmente más allá de la zona de las raíces, especialmente en suelos arenosos. Y suelos con un contenido bajo de materia orgánica.
La proporción de carbono: nitrógeno: azufre en el suelo es de aproximadamente 100:8:1. C: relaciones S de más de 300:1 puede llevar a la inmovilización.
Justus von Liebig propuso la "Ley del Mínimo" en 1862.
Descubrió, como saben los agricultores en la actualidad, que el rendimiento de las plantas suele ser limitado no sólo por los nutrientes necesarios en grandes cantidades, como el dióxido de carbono y el agua, que suelen abundar en el medio, sino por algunas materias primas como el zinc, por ejemplo, que se necesitan en cantidades diminutas pero escasean en el suelo.
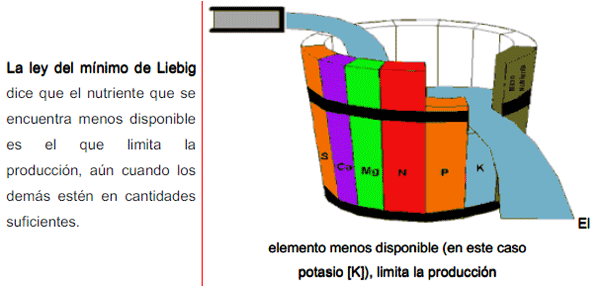
Ejemplo
Con base en esta ley, si en un suelo determinado, el nitrógeno es suficiente para producir 10 ton / ha, el fósforo es suficiente para 15 ton / ha, y el potasio es suficiente para 17 ton / ha, el rendimiento será de 10 ton / ha , EL FACTOR nitrógeno ser el factor limitante. Si el nitrógeno se añadiera para un nivel que es suficiente para 17 ton / ha, a continuación, el fósforo se convierte en el factor limitante.
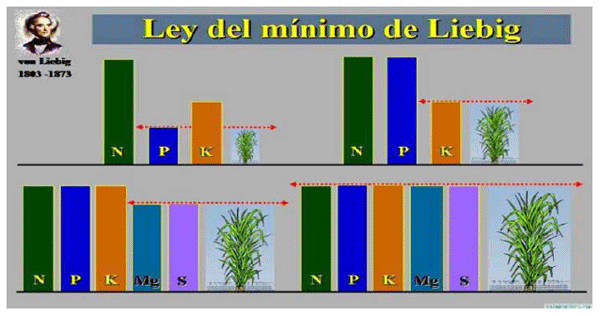
Elementos Inmobiles en el Suelo .- Concepto de Mitscherlich-Baule
Considere la posibilidad de nutrientes inmóviles como el fósforo, el zinc y potasio, la cantidad disponible para la planta depende de la extensión de la raíz. Dado que la extensión de la raíz es proporcional a la parte superior de crecimiento, la cantidad de nutrientes disponibles está estrechamente relacionado con el rendimiento de la planta. Además, dado que la extensión de la raíz puede ser afectada por las deficiencias de otros nutrientes.
PASOS ESENCIALES PARA UN PROGRAMA DE FERTILIDAD DEL SUELO CON ÉXITO
- Realizar un mapeo y recabar buenas y representativas muestras de suelo: Un análisis de suelo e interpretación sólo es tan buena como la muestra.
- Cuidado apropiado de la muestra: No contaminar la muestra. Enviar muestras inmediatamente para su análisis.
http://www.engormix.com/MA-agricultura/articulos/manejo-correccion-acidez-suelos-t5533/p0.htm
Enmiendas calizas - Corrección de suelos ácidos
1. INTRODUCCIÓN
Los suelos ácidos contienen una cantidad considerable de cationes hidrógeno. La acidificación del suelo puede ser debida a causas naturales (materia original pobre en cationes básicos, lavado de calcio en regiones de clima lluvioso, etc.) o provocada por el hombre (incorporación de residuos o fertilizantes ácidos, lluvia ácida causada por ciertas industrias, etc.).
| Clasificación de los suelos según el valor de pH | ||
| pH | Evaluación | Efectos |
| Menor de 4,5 | Extremadamente ácido | Condiciones muy desfavorables |
| 4,5 - 5 | Muy fuertemente ácido | Posibles efectos de toxicidad |
| 5,1 - 5,5 | Fuertemente ácido | Deficiente asimilación de algunos elementos |
| 5,6 - 6 | Medianamente ácido | Adecuado para la mayoría de los cultivos |
| 6,1 - 6,5 | Ligeramente ácido | El más adecuado para la asimilación de nutrientes |
| 6,6 - 7,3 | Neutro | Efectos tóxicos mínimos |
| 7,4 - 7,8 | Medianamente básico | Existencia de carbonato cálcico |
| 7,9 - 8,4 | Básico | Deficiente asimilación de algunos nutrientes |
| 8,5 - 9 | Ligeramente alcalino | Problemas de clorosis |
| 9,1 - 10 | Alcalino | Presencia de carbonato sódico |
| > 10 | Fuertemente alcalino | Poca asimilación de algunos nutrientes |
La causa más frecuente de la acidificación del suelo es el lavado del calcio en regiones con mucha pluviometría. En regiones áridas y semiáridas suele haber suficiente contenido de calcio, pero no así en las regiones muy lluviosas.
Los suelos ácidos no son favorables par el desarrollo de la mayoría de los cultivos, por lo que es preciso corregir la acidez, tratando de sustituir los cationes hidrógeno por cationes calcio. Esta operación se llamaenmienda caliza o encalado.
La función de la enmienda es la de corregir las propiedades mecánicas y físicas del suelo. La adición de cal mulle las tierras compactas.
2. ¿CÓMO SE MANIFIESTA LA FALTA DE CAL?
Ciertas observaciones permiten, antes de cualquier análisis, reconocer los terrenos provistos insuficientemente de cal.
- El estado físico del suelo- Un suelo que drena mal, que absorbe lentamente el agua de lluvia, un suelo difícil de lavar, es generalmente pobre en cal.
- La descomposición de la materia orgánica-Cuando el estiércol, los abonos verdes u otros abonos orgánicos se encuentran intactos al hacer las labores un año o más después de haberse enterrado, se pone de manifiesto que la actividad microbiana es muy pequeña, debido a un pH bajo.
- El aspecto de las cosechas y la vegetación espontánea- Cuando el trébol y, sobre todo la alfalfa vegetan, difícilmente, se puede diagnosticar el contenido insuficiente de cal en el suelo.
Los síntomas característicos de carencia de cal se localizan sobre todo en las hojas tiernas, que se tuercen en forma de ganchos. Las hojas terminales se desecan a partir de la punta y de los bordes.
La vegetación espontánea constituye también un buen índice de la acidez.
Antes de adoptar la decisión de encalar un suelo, es necesario conocer su estado cálcico. Se debe de disponer de los datos de pH y contenido en calcio (Ca2+).
| pH y contenido de calcio (Ca2+) | |||
| pH | Calcio activo | Estado cálcico | Necesidades de encalar |
| pH ≥ 6,5 | Cualquiera | Satisfactorio | No necesita encalar Control cada 2 o 3 años. |
| 5,5 < pH < 6,5 | ≥2 % ó 10 meq/100gr | Satisfactorio | Encalado de conservación |
| No satisfactorioEncalado de corrección | |||
| pH ≤ 5,5 | Cualquiera | No satisfactorio | Encalado de corrección |
a: Si el suelo es claramente ácido (pH = 5 o inferior) será necesario encalar.
- En una primera aplicación sólo se debe elevar el pH media unidad y, después, con uno o dos años de intervalo, se puede hacer otro encalado que eleva otra media unidad, hasta que el pH quede dentro del intervalo 6 a 6,5.
- No se sube más de media unidad cada vez para impedir el bloqueo de microelementos que un encalado fuerte puede producir.
- Otras razones para no subir más de media unidad son:
- Se acelera excesivamente la transformación de la materia orgánica del suelo.
- Se modifica demasiado rápidamente la vida microbiana del suelo.
- Se insolubiliza determinados elementos del suelo
- Se hace un excesivo adelanto de capital.
Con pH » 6 y tierras ligeras con alto contenido en humus no se encala porque en estas tierras un pH superior a 6,5 puede ser perjudicial.
Con pH » 6 o 6,5 y suelo arcilloso o de limo fino es conveniente encalar hasta alcanzar pH » 7. (Se busca corregir sus propiedades físicas, disminuyendo su toxicidad y haciéndolas más sueltas).
Con terreno arcilloso y cultivo de alfalfa o remolacha, no hay problema por hacer encalado y subir el pH a 7,5.
Los productos utilizados como enmienda cálcica pueden ser:
- Óxido e hidróxidos de cal.
- Carbonatos cálcicos (calizas).
- Dolomitas (carbonato cálcico magnésico)
- Sulfato cálcico (yeso).
- Margas
- Cretas
- Silicatos de calcio o magnesio.
- Residuos industriales (subproductos de azucarería)
- Cenizas de madera.
3. ENCALADO DE CORRECCIÓN
La dosis necesaria para elevar 1 Ud de pH en distintas clases de suelo y para una profundidad de 15 cm. (Si se quiere modificar 30 cm de suelo se multiplican estas cantidades por 2).
Encalado de corrección
| ||
Caliza necesaria (Kg CaCO3) para elevar el pH de:
| ||
4,5 a 5,5
|
5,5 a 6,5
| |
| Suelos arenosos |
1.500
|
2.250
|
| Suelos francos |
2.000
|
3.000
|
| Suelos limosos |
2.750
|
3.750
|
| Suelos arcillosos |
3.500
|
4.250
|
Cal viva necesaria (Kg CaO) para elevar el pH de:
| ||
4,5 a 5,5
|
5,5 a 6,5
| |
| Suelos arenosos |
850
|
1.250
|
| Suelos francos |
1.100
|
1.700
|
| Suelos limosos |
1.600
|
2.100
|
| Suelos arcillosos |
2.000
|
2.400
|
Según P.Urbano Terrón "Fitotecnia-Ingeniería de producción vegetal" se pueden utilizar distintos métodos para subir el pH de los suelos:
- Método basado en el pH y en el poder tampón del suelo.
- Método basado en el estado de saturación del complejo del complejo absorbente.
- Método de incubación.
- Método basado en el desplazamiento del aluminio de cambio.
- Método rápido basado solamente en el pH (este es el que hemos especificado o utilizado.
Poder neutralizante:
El efecto neutralizante de los diferentes productos suele referirse al de la caliza o al de cal viva tomados como índice 100.
Poder neutralizante de diferentes enmiendas
| |||
| a) Índice 100 para la caliza | b) Índice 100 para la cal viva | ||
| Cal viva CaO |
180
| Cal viva CaO |
100
|
| Cal apagada Ca(OH)2 |
136
| Cal apagada Ca(OH)2 |
76
|
| Dolomita CaCO3MgCO3 |
109
| Dolomita CaCO3MgCO3 |
61
|
| Caliza CaCO3 |
100
| Caliza CaCO3 |
56
|
| Silicato cálcico |
86
| Silicato cálcico |
48
|
| Yeso CaSO4 2 H2O |
58
| Yeso CaSO4 2 H2O |
33
|
4. ENCALADO DE MANTENIMIENTO O DE CONSERVACIÓN
Una vez conseguido el pH deseado hay que hacer un encalado de mantenimiento.
Encalado de mantenimiento
| |||
Cal viva (CaO)
Kg/ha año |
Cal apagada (Ca(OH)2)
Kg/ha año |
Cal molida
Kg/ha año | |
| Tierras ligeras |
200 – 400
|
300 – 600
|
400 – 800
|
| Tierras silíceo arcillosas |
400 – 500
|
600 – 750
|
800 – 1.000
|
| Tierras arcillosas |
500 - 600
|
750 - 850
|
1.000 – 1.200
|
Estas dosis pueden suministrarse en tierras ligeras cada 3 años, en cuyo caso habría que multiplicar las dosis anteriores por 3.
En tierras fuertes estas dosis se pueden suministrar cada 5 años, en cuyo caso habría que multiplicar las cantidades por 5.
5. FORMA DE HACER LA ENMIENDA
5.1. VELOCIDAD DE ACTUACIÓN
Las cales vivas (CaO) y apagadas (Ca(OH)2) se consideran productos de actuación rápida pues prácticamente en un mes reaccionan con el suelo y realizan su acción neutralizante.
La caliza (CO3Ca) finamente triturada es un producto de acción lenta ya que durante el primer mes solamente reacciona un 50% del producto aportado necesitándose 6 meses o más para que efectúe una acción neutralizante.
La dolomita es aún más lenta que la caliza. Resulta un 50% más lenta.
La actuación de los silicatos es excesivamente lenta por lo que son de escasa actuación.
Las espumas de azucarería y el yeso (CaSO42H2O) son de velocidad intermedia.
- Para suelos arenosos y determinados cultivos utilizar calizas (CO3Ca) y dolomitas (CaCO3 MgCO3).
- Para suelos arcillosos utilizar cal viva o apagada.
5.2. ÉPOCA DE APLICACIÓN
Se encala el suelo, no la planta. Elegir la época del año en la que se encuentren los suelos desnudos, sin cultivo. De acuerdo con la marcha de las rotaciones de los cultivos hay dos épocas muy definidas: otoño y primavera.
Normalmente se hacen aplicaciones de otoño aunque, en ocasiones, se realizan aportes en primavera. No se debe hacer aplicaciones con suelos muy húmedos para evitar pérdidas de producto.
De acuerdo con el calendario de siembras y según el producto a utilizar como enmienda, es recomendable:
- Para encalados con cal viva, anticiparse 1 mes a las fechas de siembra. Debe cuidarse la posible acción cáustica de la cal sobre las semillas.
- Para encalados con yeso o con espumas de azucarería se aportará la enmienda entre 1 y 2 meses antes de la siembra.
- Para encalados con caliza, realizar el encalado aproximadamente 3 meses antes de la siembras para que el producto tenga tiempo de actuar.
- Para encalados con dolomita, se deberá actuar con una antelación de 3 a 6 meses de la siembra.
El encalado del suelo se realizará como una operación individualizada antes de los posibles estercolados o de la fertilización de presiembra.
No debe aportarse en una vez una cantidad de enmienda que suponga una modificación de pH superior a una unidad y, siempre que sea posible, se actuará aportando cantidades menores, aproximadamente, para modificar 0,5 unidades de pH.
Observaciones:
- Si se estercola habrá que hacerlo en dos operaciones diferentes, ya que si se pone en contacto el estiércol con la cal se desprende amoníaco.
- Tampoco debe ponerse en contacto la cal con los fertilizantes nitrogenados amoniacales por los riesgos que se presentan de volatilización de nitrógeno amoniacal.
- No mezclarse con los sulfatos de cal o con las escorias fosfatadas, por existir el peligro de retrogradación de las formas asimilables de P2O5 a fosfato tricálcico, no asimilable.
- Pueden mezclarse estas enmiendas con KCl y K2SO4, pero solamente en el momento de la distribución. Sin embargo, no es práctica habitual este tipo de mezclas.
5.3. DISTRIBUCIÓN
- Si se maneja cal viva, es necesario que se apague antes de distribuirla en el campo. Para ello, se hacen montones en el suelo y se deja que se apague con la humedad atmosférica. Para impedir que se carbonate, es conveniente tapar los montones con tierra. Después se cortan los montones y se distribuyen manualmente con pala por toda la parcela.
- Si se aplica cal apagada, caliza triturada, yeso o espumas, pueden emplearse remolques o camiones distribuidores. Debe tenerse en cuenta que, debido a las elevadas cantidades a utilizar en el tratamiento, las abonadoras normalmente utilizadas en la distribución de fertilizantes minerales tienen escaso rendimiento.

5.4. ENTERRAMIENTO
Es necesario enterrar la enmienda con la ayuda de un rastra de dientes, rastra de discos o cultivador procurando que se mezcle bien con el suelo en la profundidad deseada. Generalmente, en estas operaciones se distribuye la enmienda sobre el terreno y se entierra superficialmente (15 a 20 cm) con una labor. Para una labor de mayor profundidad, se puede esperar que la cal descienda con las aguas de lluvia o de riego.
Para los cultivos polianuales como es el caso de las praderas, la aplicación se hace en cobertera utilizando productos no caústicos y aprovechando las épocas con suficiente humedad para que la cal penetre en el suelo, pero sin que las lluvias provoquen pérdidas de la enmienda.
En la práctica, para juzgar el efecto de una enmienda caliza, es necesario esperar 2 años (2 a 3 labranzas después de su incorporación) antes de tomar las muestras de tierra para su análisis.
6. CONSIDERACIONES A TENER EN CUENTA
- Las aportaciones masivas de producto efectuadas de una sola vez modifican bruscamente las propiedades del suelo, pudiendo provocar efectos desfavorables, tales como la insolubilidad de algunos elementos fertilizantes y la modificación de la vida microbiana.
- La cal, al modificar la reacción de los suelos en el sentido de basificarlos, les hace más exigentes en principios fertilizantes, contribuyendo a que se inmovilice el boro, hierro, manganeso, cobre, zinc y aluminio entre otros elementos; inmovilizado que si bien es beneficioso con relación al aluminio, no sucede otro tanto respecto a los cinco oligoelementos citados, pudiendo provocar como consecuencia carencias en los cultivos.
- En suelos arenosos es preferible utilizar dosis pequeñas repetidas frecuentemente, mientras que en suelos arcillosos pueden utilizarse dosis mayores distanciadas más tiempo.
- Una dosis excesiva en el encalado provoca una descomposición muy rápida de la materia orgánica, con lo cual aumenta el rendimiento de la cosecha durante unos cuantos años, pero a costa de agotar pronto el suelo.
- La cal agota los suelos y los buenos efectos que puede desempeñar es a costa de consumir su humus, activando su descomposición y nitrificación; por ello no deben realizarse encalados en terrenos pobres en materia orgánica a menos que se aporte ésta.
- Al incorporarse al suelo óxido, hidróxido o carbonato cálcico, una cierta proporción del producto reacciona con CO3H2 del suelo transformándose en bicarbonato cálcico soluble (CO3H)2 Ca.
- En el enyesado, el aporte es mediante sulfato de calcio. El yeso, que desempeña un papel como modificador de la potasa en los suelos, influye también muy favorablemente sobre los cultivos por el azufre que proporciona. El enyesado debe aplicarse sobre terrenos previamente bien fertilizados con productos que aporten fósforo.
- Las espumas de azucarería, que es un subproducto de la fabricación del azúcar, sirven perfectamente para ser utilizadas como enmienda caliza. Su descomposición acusa una riqueza en cal variable entre el 15% y el 30%, a la que acompañan pequeñas cantidades de ácido fosfórico, nitrógeno y potasa.
7. BIBLIOGRAFÍA
- "Manual práctico sobre utilización del suelo y fertilizantes". José Luis Fuentes Yagüe.
- "Fitotecnia-Ingeniería de la Producción vegetal". P. Urbano Terrón.
- "El suelo y los fertilizantes". J. Luis Fuentes Yagüe.
- "El suelo, los abonos y la fertilización de los cultivos". Andrés Guerrero.
- "Interpretación de análisis de suelo y consejo de abonado". Junta de Extremadura. Consejería de Agricultura, Industria y Comercio.
- "Abonos-Guía práctica de la fertilización". Andrés Gros.
- "Fertirrigación Cultivos Hortícolas y Ornamentales". Carlos Cadahía López.
Pérdida de Suelos
La pérdida imperceptible de un milímetro en el espesor de suelos cultivables sobre la superficie de una hectárea equivaldría a eliminar entre 11 y 16 toneladas de suelo agrícola fértil por hectárea. Es decir, se perderían 10 metros cúbicos de suelo fértil por hectárea. Así mismo, la pérdida de un centímetro en el espesor de suelos fértiles cultivables sobre la superficie de una hectárea, equivaldría a eliminar entre 110 y 160 toneladas de suelo agrícola por hectárea. Es decir, se perderían 100 metros cúbicos de suelo fértil por hectárea.
La erosión en suelos agrícolas es un problema cada día mayor. Los cambios climáticos globales propician variaciones en la cantidad de lluvia que en ocasiones se presenta intensamente por breves lapsos. La erosión por lluvia ó riego mal aplicado, ocasiona que muchos de los nutrientes en los suelos queden en las tierras bajas que generalmente no son cultivables porque se inundan.
Las grandes áreas de cultivo ofrecen mayor superficie para que el agua y el viento fluyan causando erosión. Los suelos sin cobertura vegetal quedan totalmente expuestos a la erosión, ya sea por agua ó viento que llevan consigo nutrientes de suelos agrícolas. Aún cuando el movimiento de suelos es un proceso natural, hay que tomar en cuenta que durante los últimos 40 años, los terrenos y las formas de cultivo han cambiado. Actualmente se cultiva en condiciones menos favorables.
La cosecha de cereales propicia que los suelos permanezcan descubiertos y expuestos a la acción de la lluvia y el viento. Así mismo, el abandono de tierras de cultivo, debido a las crisis en el campo, y a las formas de agricultura inadecuadas, deja sin materia orgánica los suelos. Ciertamente, los patrones de lluvia han cambiado en años recientes, pero no tanto como las prácticas agrícolas.
El movimiento de suelos ocasionado por lluvia y viento, trae consigo material que contiene nutrientes orgánicos e inorgánicos esenciales para los vegetales y los seres que los consumen. La pérdida de nutrientes ocurre, aún cuando el agua que corre por encima de suelos agrícolas se vea transparente y no haya clara evidencia física de erosión. Dichos nutrientes, conjuntamente con agroquímicos van a depositarse en tierras bajas y ríos.
Sabemos que, el movimiento y la erosión por lluvia, afecta más en suelos arenosos, sobretodo en aquellos con escasa materia orgánica, la cual mantiene la estructura de los suelos agrícolas. La erosión y el movimiento comienza cuando los suelos se han saturado completamente de agua, lo cual incluso puede suceder con lluvia moderada. La rapidez del movimiento es mayor en suelos arenosos, y puede empeorar en terrenos con mayor pendiente. De este modo, como resultado de la lluvia ó del riego mal aplicado, se acumula arena en las partes bajas del terreno.
Experimento
Mediante el siguiente experimento sencillo es posible conocer la cantidad aproximada de suelo que permanece en campos de cultivo:
- Ponga un puño de tierra dentro de una botella transparente y llénela con agua.2.
- Agite la botella y déjela en reposo.
- El aproximadamente 5 minutos, la arena y las piedras quedarán en el fondo de la botella.
- l agua seguirá turbia con partículas de suelos en suspensión.
- omará algunas horas para que las partículas más grandes de suelo en suspensión, se depositen en la botella sobre la arena y piedras, y algunos días para que las partículas más pequeñas de suelo se asienten en la botella.
Recordemos que las partículas de suelo contienen nutrientes de enorme importancia en la producción agropecuaria.
Reducción de Pérdidas
En la Unión Europea las siguientes medidas son populares entre agricultores y ganaderos para reducir las pérdidas y propiciar la conservación de los suelos:
- Siembra de pastos conjuntamente con cereales y entre cosechas.
- Buen sistema de drenaje para reducir la superficie disponible a erosión pluvial.
- Cobertura vegetal en los suelos para ofrecer resistencia a la erosión por lluvia y viento.
- Labranza de conservación para mejorar el drenaje y la aireación en los suelos.
- Labores de cultivo en niveles mínimos.
- Camas de siembra no demasiado finas, porque al compactar se disminuye la porosidad en los suelos y aumenta la erosión pluvial.
- Suelos cubiertos con paja u otro material vegetal residual.
Los métodos de labranza mínima ó labranza de conservación, hacen que las madrigueras de lombrices se mantengan en los suelos propiciando la existencia de materia orgánica y un mejor drenaje. Es necesario monitorear regularmente para conocer sobre la estructura del suelo y la pérdida de nutrientes, sobretodo cuando la actividad de las lombrices no es suficiente. En cultivos otoño-invierno es conveniente sembrar lo más pronto posible para asegurar que se mantenga el suelo con cobertura vegetal.
Materia Orgánica
La buena estructura en suelos agrícolas se mantiene mejor entre mayor cantidad de materia orgánica exista en ellos Esto debido a que el humus ayuda a mantener la consolidación de las partículas en los suelos, particularmente en terrenos arenosos. La incorporación de estiércol, y las prácticas de labranza mínima ó de conservación, añaden enormes beneficios a la estructura de los suelos. Los suelos se compactan debido al pisoteo del ganado y al paso de maquinaria y vehículos. En suelos compactos, el agua penetra solamente unos cuantos centímetros dentro de los suelos, sin llegar hasta donde los vegetales la requieren. Así mismo existen suelos de naturaleza compacta, cuya estructura puede ser mejorada mediante la aplicación de materia orgánica. En algunas regiones de Inglaterra, durante siglos, se ha incorporado a los suelos desperdicio de pescado, y algas marinas, como materia orgánica para conservar la fertilidad y la estructura en terrenos agrícolas.
Estiércol como Fuente de Materia Orgánica
Tipo
|
NitrógenoN
|
FósforoP2O5
|
PotasioK2O
|
CalcioCa
|
MagnesioMg
|
MateriaOrgánica
|
HumedadRelativa
|
Fresco
|
%
|
%
|
%
|
%
|
%
|
%
|
%
|
Bovinos
|
0.5
|
0.3
|
0.5
|
0.3
|
0.1
|
16.7
|
81.3
|
Ovinos
|
0.9
|
0.5
|
0.8
|
0.2
|
0.3
|
30.7
|
64.8
|
Pollos
|
0.9
|
0.5
|
0.8
|
0.4
|
0.2
|
30.7
|
64.8
|
Caballos
|
0.5
|
0.3
|
0.6
|
0.3
|
0.12
|
7.0
|
68.8
|
Cerdos
|
0.6
|
0.5
|
0.4
|
0.2
|
0.03
|
15.5
|
77.6
|
Seco
|
%
|
%
|
%
|
%
|
%
|
%
|
%
|
Bovinos
|
2.0
|
1.5
|
2.2
|
2.9
|
0.7
|
69.9
|
7.9
|
Ovinos
|
1.9
|
1.4
|
2.9
|
3.3
|
0.8
|
53.9
|
11.4
|
Pollos
|
4.5
|
2.7
|
1.4
|
2.9
|
0.6
|
58.6
|
9.2
|
Funciones del Boro en los Cultivos

El boro es un micronutriente esencial para el crecimiento y desarrollo de las plantas sanas. El boro es un elemento esencial para el desarrollo de las plantas, crecimiento, cosecha rendimiento y desarrollo de las semillas, ayudando a la transferencia de agua y la nutrición de las plantas. Aunque el requisito de boro plantas es muy baja en cantidad, su crecimiento y rendimiento de los cultivos son severamente afectados cuando existe deficiencia de boro en el suelo.
Funciones del Boro:
El boro en la división celular de las plantas: La carencia del boro dificulta el desarrollo de los ápices meristemáticos
El boro en la polinización y fructificación de las plantas: desempeña una función primordial en la formación de las anteras y en la germinación del tubo polínico, acelera la fertilización de los óvulos y reduce la caída prematura de flores y frutos.
El boro en la translocación, empleo de azúcares y otros productos del metabolismo vegetal almidón: El boro interviene en los procesos enzimáticos de síntesis de sacarosa y almidón, así como en la formación de la glucosa-6fosfato.
El boro en la resistencia de los tejidos de las plantas: Una manifestación típica de la carencia de boro es la rotura de las paredes de las células parenquimáticas, con formación de áreas necróticas, nódulos suberosos, debilitamiento del tallo, pecíolos y hojas
El boro en la fijación simbiótica del nitrógeno por las leguminosas: En situaciones de carencia de boro no se produce la formación de los nódulos activos.
El boro en la resistencia al frío, a las enfermedades y la conservación de las plantas.
El Boro es el nutriente que tiene el rango más corto entre la deficiencia y la toxicidad, pues con más de 5 ppm en el suelo se vuelve toxico. El punto crítico se encuentra en 1 ppm. Por ello que es de suma importancia el contar con el resultado de un analisis de suelo, para que junto con el dato de la meta de rendimiento a obtener del cultivo se genere con mayor precisión la fórmula de fertilización más apta para el suelo y el cultivo.
Aun después de lo antes mencionado ¿no te atreverías a realizar un analisis de suelo? Y ¿dejar fuera de la fórmula de fertilización al Boro?
El papel del Potasio en el Estrés Abiótico
Efecto del potasio sobre el estrés hídrico
El potasio del suelo llega a las raíces de las plantas gracias a la difusión y al flujo de masas; es decir, requiere de condiciones de buena humedad del suelo para poder después ser absorbido por los cultivos. En condiciones de estrés hídrico, cuando hay poca agua en el suelo por sequías, la difusión de cationes disminuye y llega poco potasio a la raíz.
Una de las consecuencias de esta deficiencia de potasio es que los estomas no cierran con rapidez, lo que genera que la planta siga transpirando y perdiendo humedad.
El potasio evita que las plantas pierdan grandes cantidades de agua mediante la transpiración en condiciones inaecuadas, esto debido a que el nutriente acelera el cierre de estomas en momentos de estrés. Este mecanismo es activado rápidamente cuando las plantas contienen buena concentración de K en sus tejidos. En Montana se realizó un experimento con cebada, en el cual se encontró que cuando las plantas tienen concentraciones altas de K, tardaron sólo 5 minutos en activar el cierre de estomas, en comparación cuando están deficientes de este nutrimento el tiempo de respuesta aumenta considerablemente.
Varias investigaciones han concluido que al tener lo que anteriormente se llamaba “consumo de lujo” de potasio, permite a las plantas responder mejor ante diversas condiciones de estrés. Es por ello muy importante que cuando se prevea un periodo de sequía, las plantas cuenten ya con un buen suministro de potasio. Mayor razón hay al aplicarlo considerando que no se corre el riesgo de una toxicidad por este nutriente.
Es importante considerar que la dinámica de absorción de potasio no es la misma en una temporada normal a una temporada con sequía. En tiempos de sequía es necesario aumentar la dosis de potasio para facilitar su disponibilidad para las plantas, recordando los mecanismos de absorción. En el cuadro 1, se presentan datos de una investigación en Iowa en la cual se encontraron menores niveles foliares de potasio en maíz con condiciones de sequía; aun en parcelas donde se fertilizó con este nutriente.
| Cuadro 1. Efecto del estrés por sequía sobre la absorción del potasio en el cultivo de maíz | ||
| Dosis de K (kg/ha) | % de potasio en las hojas | |
| Sin estrés | Con estrés | |
| 0 | 1,1 | 0,7 |
| 179,2 | 1,6 | 1,2 |
Efecto del Potasio sobre el estrés por frío (Freezing)
En condiciones de estrés por frío, también conocido como freezing, las plantas toleran mejor el cambio cuando en sus tejidos contienen buena concentración de K. Especialistas en fisiología vegetal aseguran que el suministro del nutriente antes del estrés es como adquirir un seguro para que las plantas sobrevivan en las condiciones críticas.
 En temporadas de frío el crecimiento radical decae dramáticamente, estas raíces tienen menor capacidad de absorber nutrientes, es por ello que las plantas que crecen en bajas temperaturas contienen menor concentración de K.
En temporadas de frío el crecimiento radical decae dramáticamente, estas raíces tienen menor capacidad de absorber nutrientes, es por ello que las plantas que crecen en bajas temperaturas contienen menor concentración de K.
Al igual que en condiciones de sequía, en bajas temperaturas se requiere mayor dosis de K, para evitar reducción en el rendimiento. Por ejemplo; en el cultivo de alfalfa se requiere 50% más de K en el norte de Wisconsin donde prevalecen bajas temperaturas comparado con el sur de Wisconsin con temperaturas mayores de 20 °C. Esto para lograr una concentración del 2% del nutriente en las hojas.
Además de ayudar a que las plantas toleren condiciones de estrés, el potasio proporciona los siguientes beneficios:
Mayor profundidad radical. El potasio ayuda a incrementar la capacitad de las raíces para una mejor penetración al suelo, incluso en condiciones de compactación.
Rápido crecimiento del dosel vegetal. Cuando el dosel vegetal es frondoso, la tasa de transpiración aumenta, esto significa mayor uso del agua disponible para las plantas.
Ayuda al gradiente osmótico. A mayor concentración de K en el tejido vegetal, mayor es la fuerza de atracción del agua hacia las plantas. Por lo tanto, mayor eficiencia en el uso del agua.
Maduración temprana de frutos. Un buen suministro de K ayuda a que las plantas alcancen más rápido el estado de madurez, antes que las condiciones de estrés prevalezcan.
En conclusión, el potasio es necesario en altas concentraciones en los tejidos vegetales desde etapas tempranas y de crecimiento. Una alta concentración de K en tejidos vegetales puede ayudar a tolerar condiciones adversas como sequía, bajas temperaturas, condiciones de salinidad y compactación del suelo.

Fuentes:
- Kant, S. y U. Kafkafi. 2000. Potassium and abiotic stress in Plants. The Hebrew University of Jerusalem, Faculty of Agricultural, Food and Environmental Quality Sciences, Rehovot, Israel.
- Potassium Reduces Stress from Drought, Cool Soils, and Compaction. Better crops./Vol. 82 (1998, No. 3).
Consideraciones generales sobre calidad de agua para pulverización agrícola
En Argentina existen actualmente unas 30 millones de hectáreas cultivables, si consideramos un promedio de 3 pulverizaciones por unidad de superficie, la cifra de hectáreas tratadas asciende a 90 millones por año. Sólo para el año 2009, el uso de plaguicidas asciende a 260 millones de litros/kilos, y una facturación total de 1300 millones de dólares.
Los plaguicidas (principalmente herbicidas, insecticidas y fungicidas) se asperjan con agua como vehículo de transporte. Para preservar la integridad de los fitosanitarios resulta importante promover un medio estable que no desintegre estructuralmente los principios activos, evitar que éstos queden retenidos por las cargas de partículas disueltas en el medio dispersante, y/o que ciertas reacciones químicas los inactiven. De por si el agua constituye un medio agresivo para los plaguicidas; un producto en su envase original se conserva inalterado por 36 meses, en cambio, una vez disuelto en agua su efectividad se ve comprometida en horas o días, según las circunstancias.
Los factores que influencian la calidad del agua son básicamente 5: a) el pH, una medida de la acidez o alcalinidad; b) la materia orgánica en suspensión, que provoca fenómenos de adsorción; c) partículas de arcilla (adsorción); d) la presencia de iones, cationes (calcio, magnesio, hierro y aluminio) y aniones (sulfatos, carbonatos, etc.); y e) la hidrólisis, el efecto de rotura de moléculas provocado por la cinética molecular del agua.
Efectos del pH
 El agua está constituida por dos iones hidrógeno y uno de oxígeno, se disocia en ión hidrógeno y oxidrilo, con pesos moleculares de 1 y 17, respectivamente.
El agua está constituida por dos iones hidrógeno y uno de oxígeno, se disocia en ión hidrógeno y oxidrilo, con pesos moleculares de 1 y 17, respectivamente.
La cinética química hace que sustancias disueltas en agua sufran impactos de distinta magnitud según el ión que prevalezca. La medida de la proporción relativa entre ambos se denomina pH. La escala tiene un rango entre 0 y 14; un valor de 7 es la neutralidad, que se interpreta como la misma cantidad de hidrógeno y oxidrilo. Valores menores a 7 son ácidos (mayor cantidad de hidrógeno), y mayores alcalinos (mayor cantidad de oxidrilos). Ejemplos cotidianos son las gaseosas cuyo valor de pH es 3, y soluciones de lavandina con valores próximos a 10-11. Una gaseosa constituida por azúcares se puede conservar en una góndola sin ser atacada por bacterias por la acidez de la solución conferida por el gas carbónico; y una mancha es quitada de una prenda gracias a la destrucción del colorante por el elevado pH conferido por la lavandina.
Concluimos entonces que, en general, el pH ácido conserva y el alcalino destruye. El pH neutro no es el mejor valor para que un agua conserve la integridad de los pesticidas, en la generalidad de los casos un valor ideal se encuentra entre pH 4 y 6 para casi todos los productos. Si nuestra intención es destruir residuos de plaguicidas debemos subir el pH utilizando soluciones de lavandina u otros productos alcalinos.
Hasta aquí describimos cualitativamente los efectos, pero es necesaria una medida cuantitativa de la calidad del agua. Ya que el pH es la inversa del logaritmo de la concentración de iones hidrógeno (pH= log 1/ [ H+ ]), cabría preguntarse cuánto menos agresiva es un agua de pH 4 respecto a otra de pH 8?. Repasando conceptos básicos aritmética (cuarto año del Colegio Nacional), sabemos que log 10.000=4 y log 1000=3; deducimos entonces que cuando el pH se reduce en 1 unidad, la cantidad de oxidrilos es 10 veces menor. Para el ejemplo expuesto, bajar el pH de 8 a 4, la cantidad de oxidrilos se reduce 10.000 veces (=10x10x10x10).
 La interpretación es que ahora el medio tiene 10.000 veces menos probabilidad de colisionar a nuestra molécula de plaguicida con una masa grande (oxidrilo), y por ende se incrementa la probabilidad de su conservación. Si ese plaguicida fuese Glifosato, su masa es 170 g, o sea, unas 10 veces más grande que el agua. El Glifosato es extremadamente sensible a la reacción del agua.
La interpretación es que ahora el medio tiene 10.000 veces menos probabilidad de colisionar a nuestra molécula de plaguicida con una masa grande (oxidrilo), y por ende se incrementa la probabilidad de su conservación. Si ese plaguicida fuese Glifosato, su masa es 170 g, o sea, unas 10 veces más grande que el agua. El Glifosato es extremadamente sensible a la reacción del agua.
Un ejemplo de dicha sensibilidad al pH lo constituye este ejemplo control químico del sorgo de Alepo con una dosis baja de 1.5 lt/ha de Glifosato (fuente: Ing. Agr. Agustín Mitidiieri). Con pH de 8 el control es 20%, utilizando un corrector y bajando el pH a 5 (unas 1000 veces menos oxidrilos) el control se eleva a 90%.

Ejemplos para insecticidas lo constituyen el caso del fosforado Clorpirifós y el piretroide Cyflutrin. Puede apreciarse como la vida media del fosforado se incrementa sustancialmente de 1 a 35 días cuando el pH baja de 8 a 7; y como el piretroide lo hace desde 1, 20 y 120 días cuando se modifica el pH desde 9, 7 y 4 respectivamente.

Se entiende por vida media el tiempo para reducir la concentración del activo un 50%. Se aprecia como el efecto del pH está influenciado por la molécula del plaguicida; distintos principios activos tienen diferente sensibilidad.
Turbidez del agua
Los sólidos disueltos en agua le quitan transparencia. A pesar de trascurrir el tiempo el agua permanece turbia, ya que las partículas en suspensión poseen cargas de igual signo (negativo) y se repelen. Esas cargas son las que adsorben a los plaguicidas (retienen moléculas en su superficie). La magnitud de ese efecto se conoce como capacidad de intercambio catiónico (CIC [meq/100 g suelo seco]), con valores promedio de 300 para la materia orgánica, 100 para arcilla y 10 para el limo.
 Si nosotros agregamos un ácido al agua turbia, neutralizamos las cargas y los sólidos precipitan, tal como ilustra la fotografía (izquierda).
Si nosotros agregamos un ácido al agua turbia, neutralizamos las cargas y los sólidos precipitan, tal como ilustra la fotografía (izquierda).
El gráfico de la derecha ilustra una experiencia de control de sorgo de Alepo con un agua conteniendo materia orgánica (barras de la izquierda). Con un pH de 5.8 el control de la maleza es sólo del 40% (rojo); cuando bajo el pH a 4.4 mediante el uso de un corrector, el control supera el 80% (amarillo). El corrector neutralizó los sólidos, se redujo la adsorción del Glifosato, y como consecuencia hubo mayor disponibilidad del herbicida para controlar la maleza.
Queda claro entonces que, el uso de aguas turbias afecta la performance del Glifosato (en casos que la turbidez se deba a arcilla o materia orgánica), y esta práctica es habitual en trabajos de pulverización. Por ende se recomienda acidificar el agua almacenada en las cisternas de apoyo cuando provienen de fuentes sucias. Complementariamente, es recomendable que el fondo del tanque tenga un plano inclinado y disponga de un robinete de manera tal que, cuando se desaloja parte del agua se arrastren los sedimentos y eliminen del depósito. Igualmente, y como medida de precaución, abastecer el pulverizador tomando el agua desde un nivel superior al fondo.

Dureza del agua
Se denomina dureza a la concentración de iones de calcio y magnesio (Ca+ y Mg+) expresada en mg/lt, unidad equivalente a partes por millón (ppm). En la práctica las aguas duras son las que generan sarro en los recipientes para hervir agua. Los valores críticos de pH de las aguas duras rondan entre pH 7.5 y 8.2. La mejor forma de determinar dureza es mediante un análisis físico-químico del agua. En el último gráfico (barras de la derecha) demuestra que cuando el agua es blanda, las correcciones de pH no inciden en los resultados de control.
Dado que la dureza es dada por la concentración de dos cationes, se la suele expresar en equivalente a carbonato de calcio (CaCO3), y ese valor recibe la denominación de dureza total. Así por ejemplo, un agua con 285 ppm de Ca y 131 ppm de Mg, tiene una dureza total de 1237 ppm CaCO3 (=2.5 x 285 + 4 x 131).
Particularmente para Glifosato, la dureza del agua le produce una fuerte inactivación parcial del principio activo, y reduce consecuentemente los porcentajes de control; notable para aquellas malezas de difícil control (e.g. gramón Cynodon dactylon, Capín - Cola de Zorro Setaria spp., Cebollín Cyperus rotundus,Ocucha Parietaria debilis).
Una fórmula permite cuantificar el proceso (Villaseca, S.; 1988):
Inactivación (%)= V (LpH) * Dureza (ppm CaC03) * 47 10-5 / Dosis sal (kg/ha)
Dicha fórmula señala que para reducir la inactivacón de Glifosato (cuando trabajamos con aguas duras) resulta conveniente reducir el volumen de aspersión, utilizar aguas de baja dureza total o incrementar las dosis del herbicida. Un ejemplo práctico permitirá cuantifica la inactivación. Ejemplo: dureza total= 300 ppm CaCO3, dosis= 1 kg de sal isopropil amina (equivalente a 2 lt/ha de Gifosato 48%) y un volumen variable de 100 y 300 lt/ha (habituales para cultivos de soja y papa, resp.). A continuación una interpretación de dureza.
| Dureza como ppm CaCO3 | Interpretación |
0 - 75
|
blanda
|
75 - 150
|
semidura
|
150 - 300
|
dura
|
> 300
|
muy dura
|
Aplicando la fórmula, los porcentajes de inactivación resultantes son 14.1 y 42.3%, para el menor y mayor volumen respectivamente. La consecuencia es un efecto de 1.7 y 1.15 lt/ha de Glifosato activo. Muchas veces se observan mejores controles de malezas cuando son pulverizadas con avión respecto a los tratamientos terrestres, debido a que las mismas dosis pulverizadas con 10 lt/ha de caldo sólo inactivan el 1.4% del herbicida (comparando 10 vs 100 lt/ha).
La pregunta consecuente es: ¿ qué porcentaje de inactivación está Ud. dispuesto a tolerar ? Un valor aceptable es 7-10%, compatible con la tolerancia del caudal de las pastillas de aspersión. Luego: ¿ con qué dureza del agua resulta necesario utilizar correctores ?. Siguiendo este razonamiento, y sobre la base de un volumen de 100 lt/ha con equipo terrestre, la calidad del agua como límite de dureza sería 150 ppm de CaCO3. Inmediatamente surge otra pregunta: ¿Y si lo hago con avión? La respuesta resulta evidente: 1500 ppm de CaCO3, para lograr el mismo efecto de inactivación. De cualquier manera, los fenómenos se interrelacionan; un menor volumen implica una mayor concentración de dosis, y por ende una difusión más rápida del plaguicida en la hoja de la maleza, que finalmente se traduce en una mayor dosis absorbida.
Corrección de dureza
Las sales de calcio y magnesio actúan como secuestrantes. En consecuencia deben ser neutralizadas, o eliminadas, como paso previo al agregado del herbicida. Debe quedar claro que la corrección del agua es un paso previo al agregado de Glifosato al pulverizador.
Existen dos caminos posibles: eliminar las cargas de los cationes (quelatarlos) o, sacar los iones de la solución o caldo de aspersión. La segunda opción se detalla en el siguiente gráfico.

Nuevamente, recurriendo a los conocimientos de química general e inorgánica (cuarto año del Colegio Nacional), vemos que el sulfato de amonio es una sal de ácido fuerte y base débil, que se disocia en anión sulfato y catión amonio. Se trata de una sal de color marrón de baja solubilidad. El calcio se combina con el anión sulfato dando sulfato de calcio (=yeso), una sal insoluble que precipita en forma irreversible, quitando al calcio de la solución.
El catión amonio es muy soluble y se combina con el Glifosato, actuando como carrier o trasportador, incrementando notablemente la velocidad de absorción del herbicida (aumenta la dosis total absorbida por la maleza).
Existen en el mercado productos específicos formulados como soluciones, dada la dificultad de disolver la sal de sulfato de amonio, más el inconveniente que genera el precipitado de la sal que se forma (sulfato de calcio). Dicho producto es un quelato de sulfato de amonio al 40%, y se recomienda a dosis entre 2 y 3 lt por cada 100 lt de caldo.
Se destaca que el sulfato de amonio líquido es efectivo para control de malezas difíciles aún para aguas de baja dureza, tanto por el efecto acidificante del sulfato residual, como por la presencia del amonio, que acelera la absorción.
Observaciones importantes
Si bien existe instrumental portátil para realizar análisis de aguas resulta importante hacer un análisis en un laboratorio especializado. La toma de la muestra debe realizarse siempre del caño de abastecimiento y no del tanque; dejando correr el agua y lavando varias veces el recipiente. Utilizar envases plásticos que hayan contenido agua mineral para evitar contaminantes.
La época del año más adecuada es el verano, donde previamente no hayan ocurrido lluvias abundantes; esta época asegura la mayor concentración salina y los mayores valores de pH. La calidad del agua varía mucho en cortas distancias, por ende se recomienda analizar todas las fuentes disponibles de un campo. Se debe solicitar un análisis físico-químico completo, que es de bajo costo relativo, en función de los valores de los plaguicidas.
Un agua dura presenta habitualmente valores de pH próximos a 8 y nunca superiores a 8.5, que indicarían la presencia de sodio. El agua puede ser salina o muy salina, pero de pH neutro. Muchas veces secuestrando cationes alcalinos térreos el valor de pH baja, otras veces no. Por eso no utilizar correctores de efecto combinado, sin conocer previamente el factor limitante.
Cada plaguicida tiene un valor de pH óptimo, para conservar el principio activo; como promedio podemos considerar un valor de pH=5. Para una mayor precisión consulte con un especialista o al fabricante del plaguicida.
El agregado de coadyuvantes, correctores de pH y/o secuestrantes, debe hacerse previo a la incorporación de los plaguicidas. No olvidar además, que las reacciones químicas llevan tiempo. Resulta una paradoja que un agua de pH 8, una vez incorporado Glifosato el valor baja a 4, a expensas del herbicida. Destacamos la importancia de repetir que el primer paso es corregir el agua. Este trabajo podría realizarse el día anterior o, en el tiempo que media entre que el equipo sale a pulverizar el lote y regresa a recargar (unos 45 minutos).
Prepare el caldo de aspersión lo más próximo posible a su aplicación. El agua es el peor enemigo de los plaguicidas, produce hidrólisis (hidro= agua; lisis= rotura). Si por cualquier motivo debe interrumpir una pulverización, acidifique el caldo residual, utilizando un corrector de pH.
Sin el afán de ofender y solo de apoyar. Sus publicaciones serian mas serias y de mayor importancia y agregara bibliográfica. Saludos
ResponderEliminarUn artículo muy detallado y completo. Es de suma importancia conocer la calidad del suelo para saber qué tipo de plantas pueden crecer en él; además, se está llevando a cabo un estudio de la biosolarización en Argentina, que consiste en la preparación del suelo gracias a la energía del sol.
ResponderEliminar